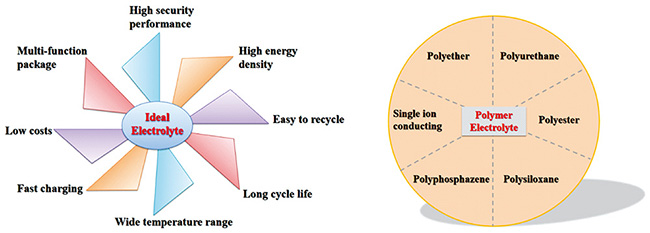
1 引言
表1 全固态电解质的优势Table 1 Solid state battery advantage |
| Index | Performance |
|---|---|
| High theoretical energy density | Key indicators can reach 300~400 Wh/kg |
| High security performance | Replacing electrolytes and separators in traditional lithium-ion batteries with solid electrolytes |
| Wide operating temperature range | -25 ℃~-60 ℃ |
表2 目前商业化的全固态电解质的研究情况Table 2 Research status of commercialized all-solid electrolytes |
| All solid state battery research and development organization | Type of battery | Key indicator | Battery capacity | Application status |
|---|---|---|---|---|
| Batscap-Bolloré | Li/PEO/LFP | 220 Wh/kg,1500 cycle,96% | 10~30 Ah | Successfully applied to the French EV shared service car “Autolib” and the small bus “Bluebus”, the car currently has more than 4,000 vehicles. |
| Sakti3 | Li/LiPON/LCO | 1000 Wh/L | 10~50 mAh | Special field application. |
| Toyota | Li/LPS/LCO Li/LPS/NCM | 230 Wh/kg | 2.4~15 Ah | Small flatbed trial phase. No large-scale promotion. Expected listed in 2022. |
| Qingdao Institute of Energy, Chinese Academy of Sciences | Li/LLZO@PEO/NCM | 297 Wh/kg | 10 Ah | Development phase |
| Ningbo Institute of Materials, Chinese Academy of Sciences | GP/Oxide solid electrolyte/NCM | 240 Wh/kg, | 500 cycle, 88.7% 4 Ah | Pilot line construction is underway |
| Qing Tao | GP/Oxide solid electrolyte/NCM | 220 Wh/kg, 1000 cycle | 5.6 Ah | Pilot line construction is underway |
| Weilan New Energy | Silicon carbon anode @Li/in situ solid state Electrolyte/NCM | >300 Wh/kg | 1.8~42 Ah | Pilot line construction is underway |
| Solid Power | Li/LPS/S | 300 Wh/L | 1~5 Ah | Development phase |
表3 全固态电解质的汇总Table 3 Summary of all solid electrolytes |
| Classification | SPE | Ionic conductivity (S/cm) | Electrochemical window(V) | Thermal decomposition temperature(℃) | ref |
|---|---|---|---|---|---|
| Polyether | PEGBCDMA/EC/LiTFSI | 8.0×10-4, RT | 4.5 | 220 | 8 |
| CCPL | 3.0×10-4, 60 ℃ 1.4×10-3, 160 ℃ | 4.6 | — | 47 | |
| PEO/PEI/LiClO4 | 1.0×10-4, RT | — | — | 48 | |
| LiFSI/PEO | 1.3×10-3, 80 ℃ | 5.3 | — | 49 | |
| PEO/LLZTO/PEG | > 10-4, 55 ℃ 1.58×10-3, 80 ℃ | 5.0 | — | 50 | |
| PVDF-HFP-Li6.5La3Zr1.5Ta0.5O12 PVDF-HFP-Li6.4La3Zr1.4Nb0.6O12 | 8.8×10-5, RT 6.8×10-5, RT | — | — | 51 | |
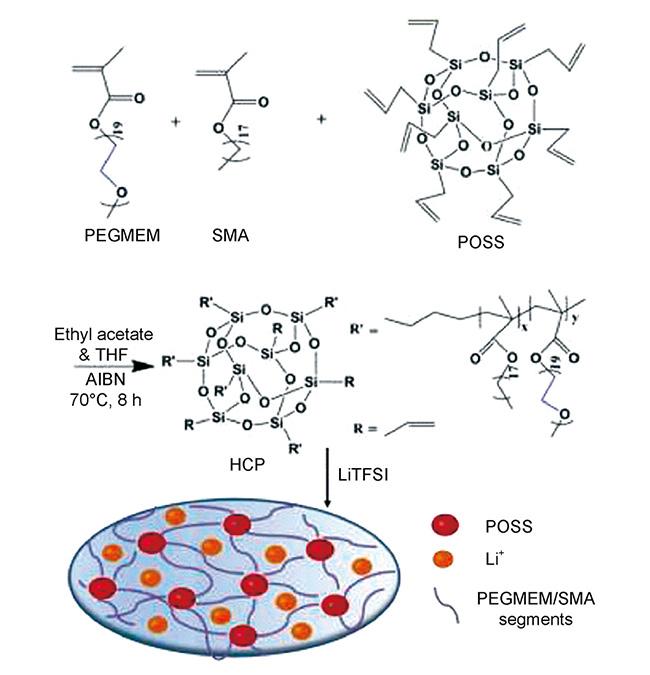
| 5 wt% POSS/HPE | 1.39×10-3, 80 ℃ | 5.0 | 298 | 52 | |
| PMHSnC-B | 1.0×10-3 , RT | 4.5 | 500 | 53 | |
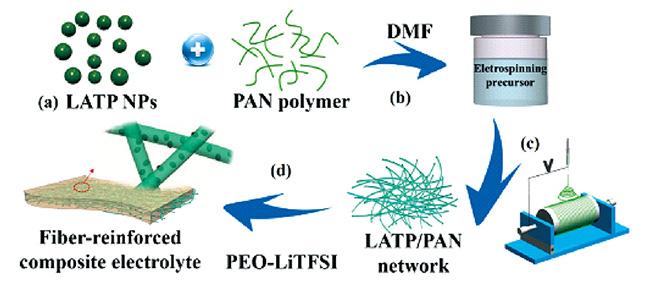
| LATP/PAN/PEO-LiTFSI | 6.5×10-4, 60 ℃ | 5.0 | — | 58 | |
| 5 wt%LLZO/PAN-LiClO4 | 1.31×10-4, RT | — | — | 59 | |
| Polyester | 10 wt% PVDF/90 wt% [EMI][TFSI] | 4.9×10-3, 60 ℃ | — | — | 64 |
| C-PEGDE | 8.9×10-5, RT | 4.5 | — | 66 | |
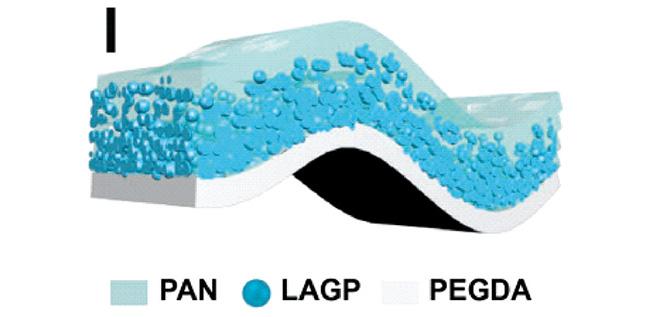
| PAN/LAGP/PEGDA | 3.7×10-4, RT | 5.0 | — | 67 | |
| PFCA-CPE | 1.24×10-3, RT | 5.0 | — | 68 | |
| PPC/Li6.75La3Zr1.75Ta0.25O12 | 5.2×10-4, 20 ℃ | 4.6 | — | 70 | |
| PCL | 4.1×10-5, 25 ℃ 1.1×10-4, 40 ℃ | — | — | 71 | |
| CPPC | 3.0×10-4, 20 ℃ 1.4×10-3, 120 ℃ | 4.6 | — | 72 | |
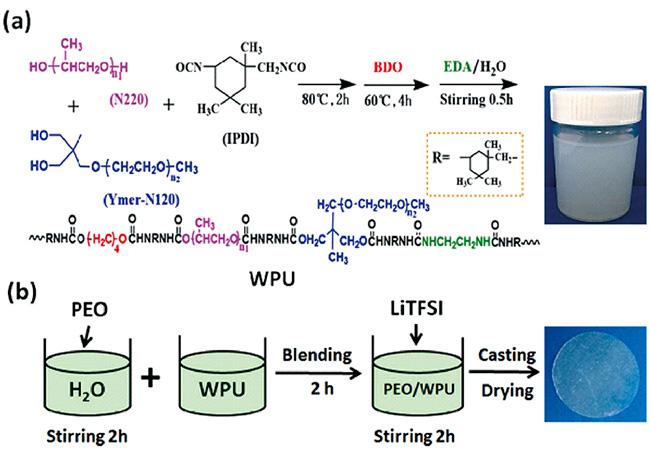
| Polyurethane | PEO/WPU/LiTFSI | 8.2×10-4, 60 ℃ 3.1×10-3, 80 ℃ | 4.8 | 336 | 76 |
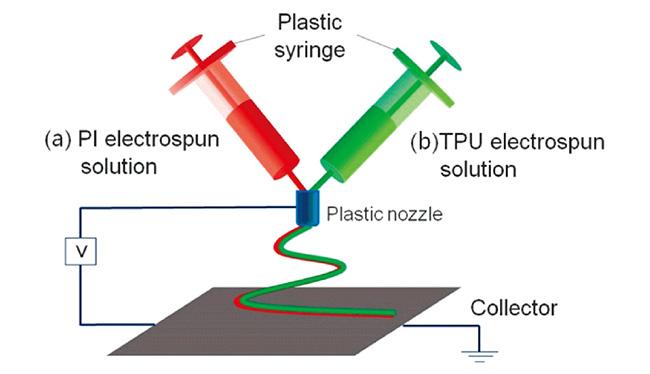
| TPU/PI | 5.06×10-3, RT | — | — | 77 | |
| SiO2 /PEI-PU | 2.33×10-3, RT | — | — | 79 | |
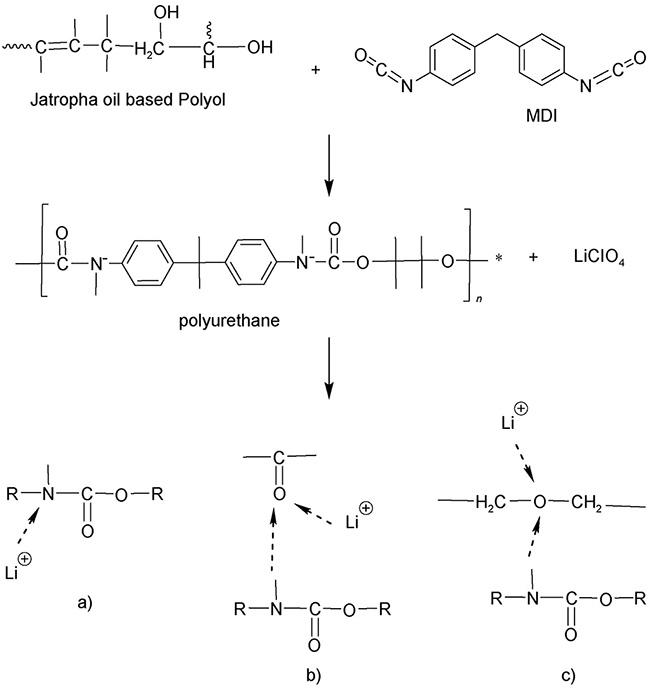
| PU/MDI/LiClO4 | 1.29×10-4, 30 ℃ | 4.8 | 80 | ||
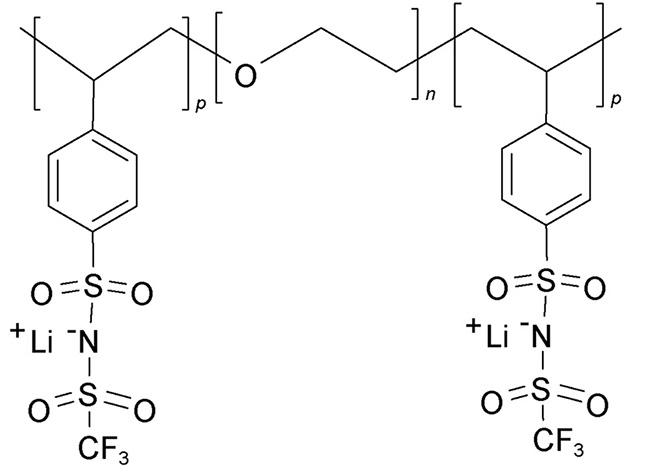
| Single ion conducting | P(STFSILi)-PEO-P (STFSILi) | 1.3×10-5, 60 ℃ | 5.0 | — | 54 |
| LiPSsTFSI/PEO | 1.0×10-4, 70 ℃ | — | — | 16 | |
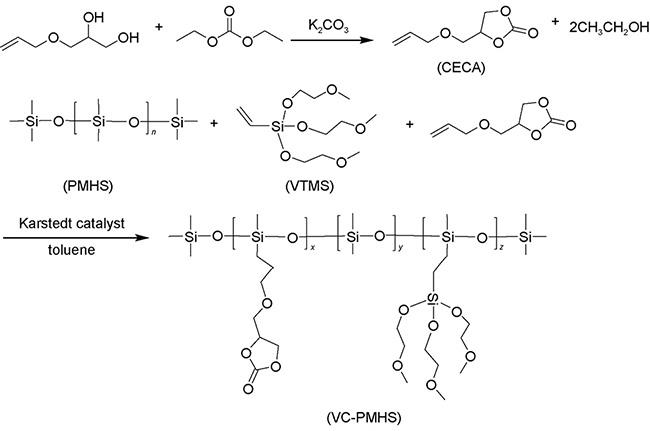
| Polysiloxane | VC-PMHS | 1.55×10-4, 25 ℃ | — | — | 87 |
| 1.5×10-3, 100 ℃ | |||||
| Polysiloxane/Polyether-based | 1.5×10-4, RT | — | — | 90 |
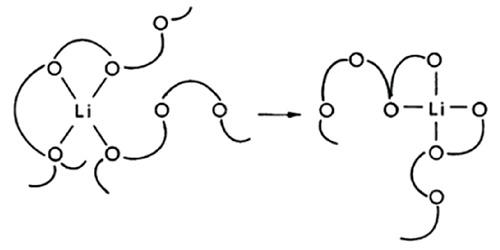
2 全固态聚合物电解质理论
3 全固态聚合物电解质
 O、—S—、—N—等,有助于盐的解离作用;③聚合物应具有通道,能使锂离子发生迁移运动,并且根据常见的导电机理,链段上最好有高的柔顺性以及低的键旋转能垒,这能有助于链段运动;④聚合物应有较好的热学和力学稳定性,可以抑制锂枝晶的生长并且有多加工性能。
O、—S—、—N—等,有助于盐的解离作用;③聚合物应具有通道,能使锂离子发生迁移运动,并且根据常见的导电机理,链段上最好有高的柔顺性以及低的键旋转能垒,这能有助于链段运动;④聚合物应有较好的热学和力学稳定性,可以抑制锂枝晶的生长并且有多加工性能。3.1 聚醚
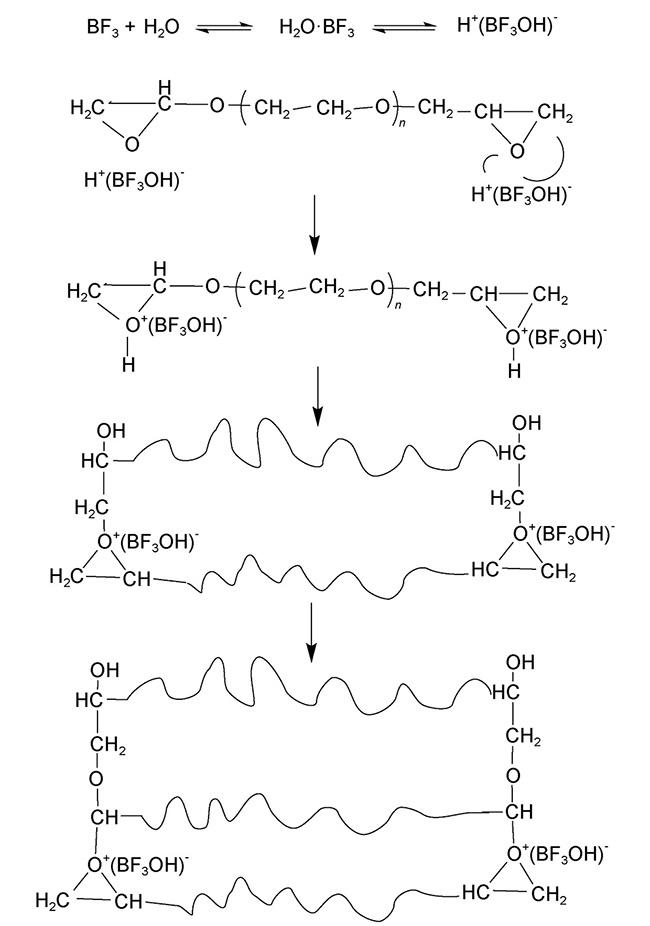
3.2 聚碳酸酯
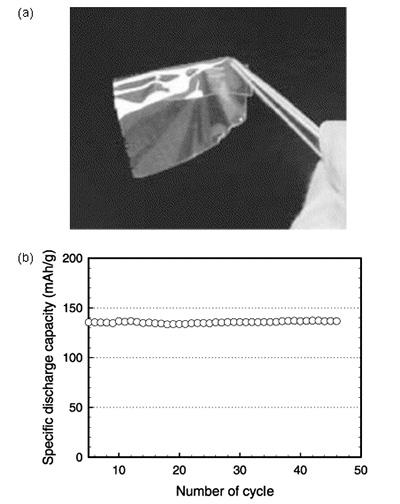
图11 (a)软包电池运行良好时和(b)软包电池被切除一个小角后给LED灯供电;(c)缺角软电池的电压检测;(d)切下来的小角给LED灯供电[71]Fig. 11 Illustration of solid-state soft-package lithium cells(a) On the well-running and (b) Being cut away for powering a red LED lamp; (c) Voltage monitoring of obtained incomplete battery; (d) The obtained corner of the cell for lighting a LED lamp[71]. Copyright 2015, Wiley |
3.3 聚氨酯
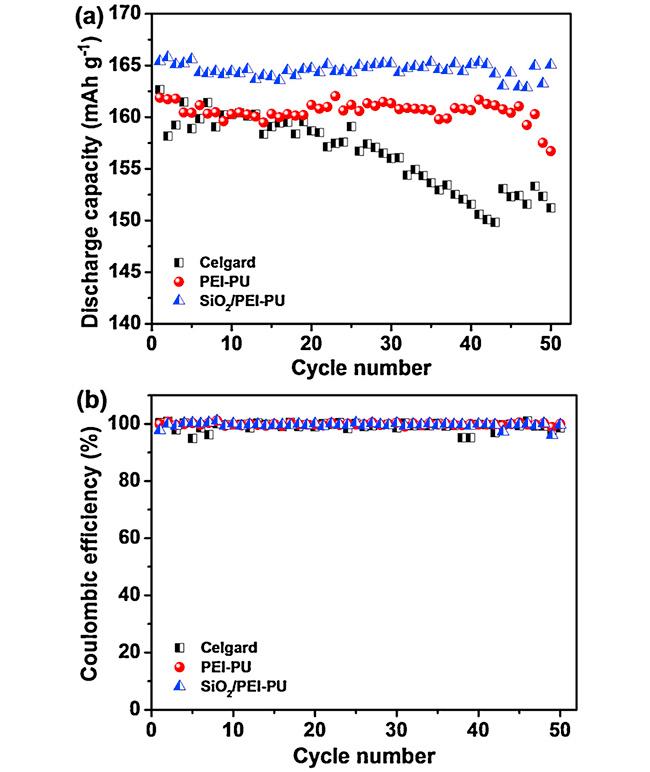
图14 (a)Celgard,PEI-PU和SiO2/PEI PU复合膜的Li/LiFePO4电池以0.2 C速率的循环稳定性;(b)Celgard,PEI-PU和SiO2/PEI PU复合膜以0.2 C速率的库仑效率[78]Fig. 14 (a) Cycling stabilities of Li/LiFePO4 cells using Celgard, PEI-PU and SiO2/PEI PU composite membranes at 0.2 C rate. (b) Coulombic efficiency as a function of cycle number at 0.2 C rate[78]. Copyright 2015, Elsevier |
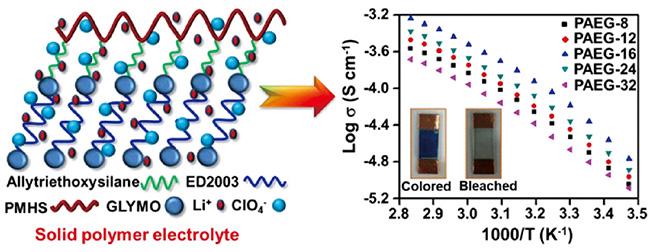
3.4 聚硅氧烷
4 结论与展望
 O)—O—]具有较高的介电常数,因而较PEO电解质而言,PC电解质应具有更高的离子电导率。改性后拥有众多的优异性,例如耐热性、耐高压性和充放电性能强等,但是离子电导率仍需要进一步提高,因此,仍然需要根据分子各自的特性,设计合成更多性能优异的复合材料。
O)—O—]具有较高的介电常数,因而较PEO电解质而言,PC电解质应具有更高的离子电导率。改性后拥有众多的优异性,例如耐热性、耐高压性和充放电性能强等,但是离子电导率仍需要进一步提高,因此,仍然需要根据分子各自的特性,设计合成更多性能优异的复合材料。