1 引言
2 硝酰氯的源和汇
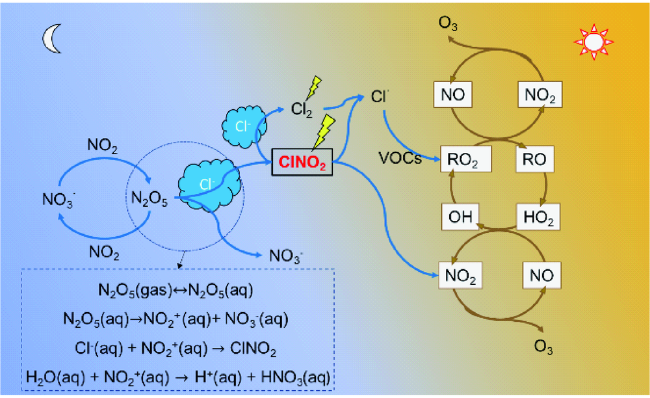
2.1 来源机制
2.2 去除机制
3 测量技术
3.1 直接测量技术
3.2 间接测量技术
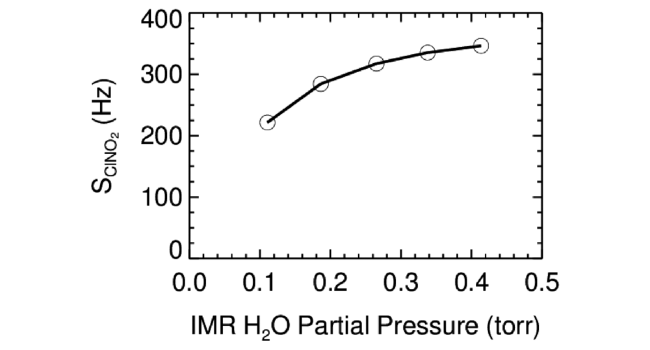
3.3 硝酰氯测量的标定
4 硝酰氯的分布特征和环境影响
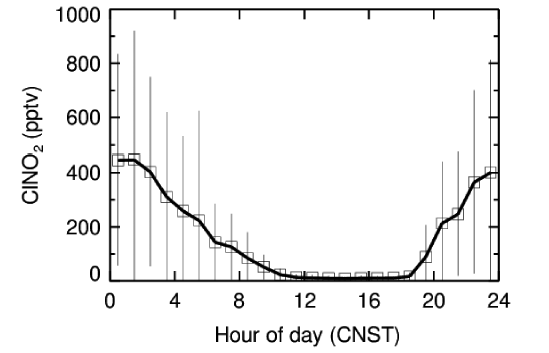
4.1 时空分布特征
表1 文献报道的国内外外场观测ClNO2浓度以及ClNO2产率的结果汇总Table 1 Summary of the results of field observations of ClNO2 concentration and ClNO2 yield reported in the literatures |
| Location | Region | ClNO2 (ppb) (max, mean) | ClNO2 yield (range, points) | ref |
|---|---|---|---|---|
| Wangdu, CN | Rega | 2.07, 0.55 | 0.06~1.04 (10) | 24 |
| Jinan, CN | Urban | 0.78, 0.09±0.06 | 0.01~0.08 (4) | 37 |
| Mt Tai, CN | RLb | 2.1, 0.05±0.11 | 0.17~0.90 (8) | 46 |
| Beijing, CN | Urban | 1.4, 0.17±0.26 | 0.10~0.35 (4) | 36 |
| HK, CN | Coastal | 4.7, n.a. | 0.02~0.98 (9) | 47 |
| Beijing, CN | Rural | 2.9, 0.8 | 0.5~1.0 (5) | 48 |
| Seoul, KOR | Urban | 2.5, n.a. | n.a. | 49 |
| Seoul, KOR | Rega | 0.8, n.a. | n.a. | 49 |
| London, UK | Urban | 0.72, n.a. | n.a. | 31 |
| Calgary, CA | Rural | 0.34, 0.04 | 0.005~ 0.12 | 25 |
| KFd,GER | Rural | 0.7, n.a. | 0.035~1.38 (33) | 39 |
| North Coast, UK | Coastal | 0.065, 0.01 | n.a. | 40 |
| BC, Canada | Coastal | 0.1, 0.008 | 0.7 (1) | 50 |
| UK | Lc | 4.1, 0.9 | n.a. | 41 |
| Mediterranean | Coastal | 0.439, 0.02 | 0.53 (1) | 38 |
| Suez | Coastal | 0.586, 0.075 | 0.90 (1) | 38 |
| Red Sea | Coastal | 0.480, 0.047 | 0.86 (1) | 38 |
| Aden | Coastal | 0.379, 0.041 | 0.76 (1) | 38 |
| Arab. Sea | Coastal | 0.056, 0.007 | 0.87 (1) | 38 |
| Oman | Coastal | 0.376, 0.067 | 0.50 (1) | 38 |
| Arab. Gulf | Coastal | 0.126, 0.021 | 0.17 (1) | 38 |
| Houston, US | Coastal | 1.2, n.a. | 0.1~ 0.65 (2) | 3 |
| Boulder, US | Rural | ~0.45, n.a. | n.a. | 4 |
| LA, US | Urban | 2.15, n.a. | n.a. | 43 |
| Boulder, US | Rural | 1.3, 0.27 | 0.45~0.8 (2) | 42 |
| Weld, US | Rural | n.a., 1.2±0.7 | 0.05~0.90 (85,440) | 51 |
| Calif, US | Urban | 3.6, n.a. | n.a., n.a. | 44 |
| Houston, US | Urban | 0.1, n.a. | n.a. | 32 |
| Eastern, US | RLb | n.a., n.a. | 0.003~1 (3425) | 52 |
*aReg: Regional;bRL: Residual layer;cL: Landfill;dKF: Kleiner Feldberg |
4.2 硝酰氯的非均相生成和产率
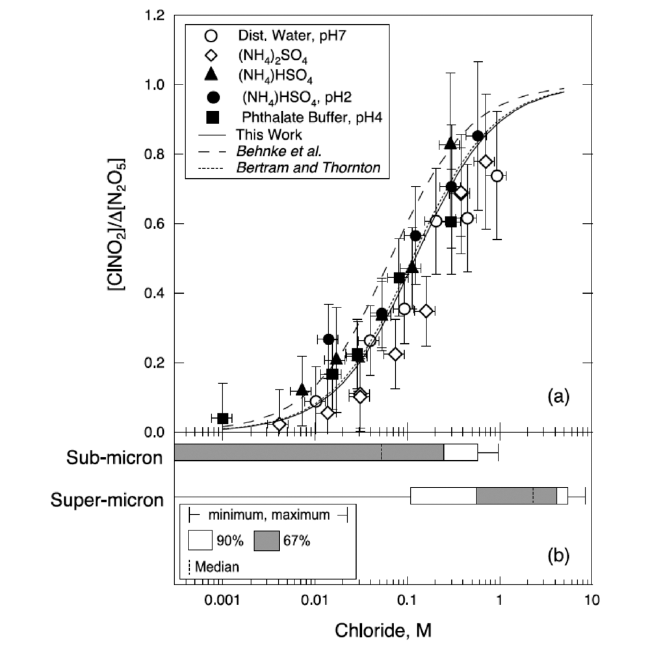
图6 (a)实验室定量的ClNO2产率与颗粒物中Cl-物质的量的响应关系(摘自文献[8]图3, 版权归属于John Wiley and Sons);(b)2016年墨西哥湾TexAQS-GoMACCS外场观测期间测得的亚微米和超微米颗粒物中氯离子的浓度范围Fig.6 (a) The efficiency of conversion of N2O5 to ClNO2 as a function of substrate chloride concentration, and (b) the range of sub- and super-micron chloride concentrations measured during the TexAQS-GoMACCS 2006 field study in the Gulf of Mexico (original figure referred from[8], copyright: John Wiley and Sons) |
4.3 硝酰氯化学的环境效应
表2 已有观测中ClNO2贡献Cl·生成速率日间峰值汇总Table 2 Summary of the campaign average daily peak of the chloride radical via ClNO2 photolysis reported in previous filed campaigns |
| Location | Region | P(Cl·) (×105 cm-3·s-1) Mean diurnal peak | ref |
|---|---|---|---|
| Hong Kong, CN | Coastal | 3.1 | 64 |
| Wangdu, CN | Regional | 16.3 | 24 |
| Beijing, CN | Rural | 5.2 | 30 |
| Hessen, GER | Rural | 12 | 63 |
| London, UK | Urban | 2.5 | 31 |
| Calgary, CA | Rural | 7 (Campaign peak) | 25 |
| Norfolk Coast, UK | Coastal | <1.0 | 40 |
| Houston, US | Urban | 8.0 | 3 |
| Boulder, US | Rural | 2.5 (Estimated) | 4 |
| Los Angeles, US | Urban | 25 | 53 |
| Houston, US | Urban | 3.4 (Estimated) | 32 |