Contents
1 引言
2 Cs2CO3辅助钯催化C—H官能团化
2.1 Cs2CO3辅助钯催化C(sp2)—H官能团化
2.1.1 Cs2CO3直接辅助钯催化C(sp2)—H活化
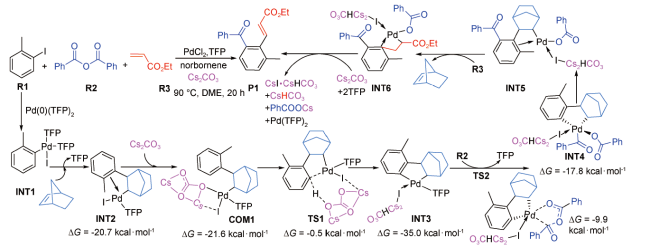
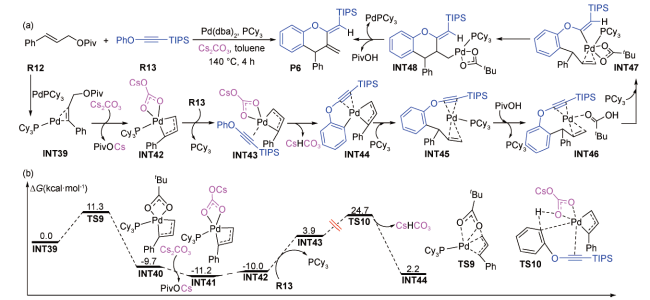
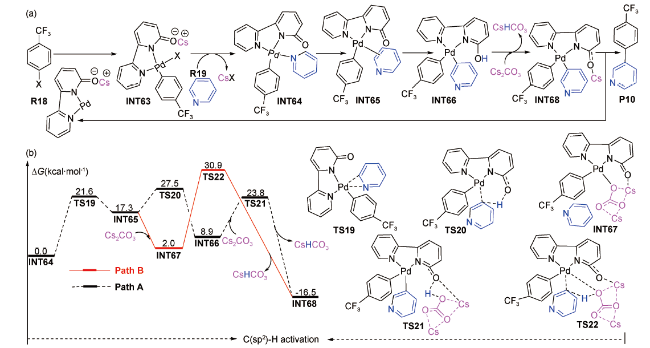
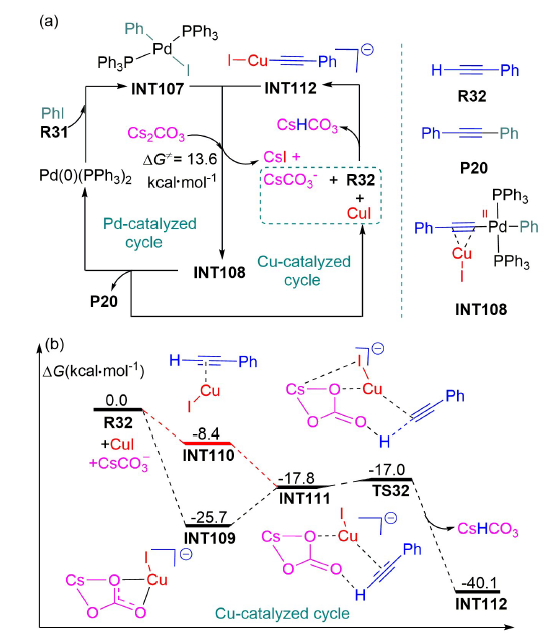
图式7 Cs2CO3辅助钯催化苯基三异丙基甲硅烷基乙炔基醚与新戊酸肉桂酯双C—H裂解的环化反应机理(a)及其芳基C(sp2)—H活化的势能剖面图(b)[78]Scheme 7 (a) Reaction mechanism for Cs2CO3-assisted palladium-catalyzed double C—H cracking and cyclization of phenyl triisopropylsilyl ethynyl ether with cinnamyl pivalate, and (b) potential energy profiles for aryl C(sp2)—H activation[78] |
2.1.2 Cs2CO3间接辅助钯催化C(sp2)—H活化
2.2 Cs2CO3辅助钯催化C(sp3)—H官能团化
2.2.1 Cs2CO3直接辅助钯催化C(sp3)—H活化
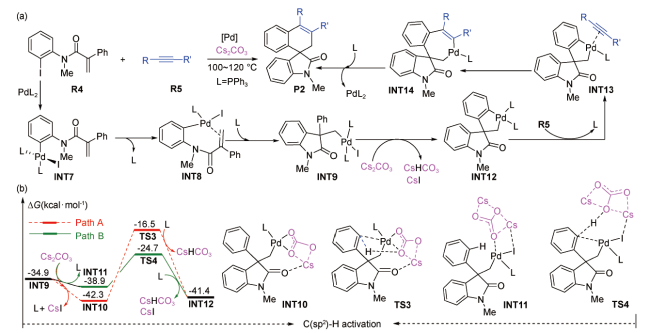
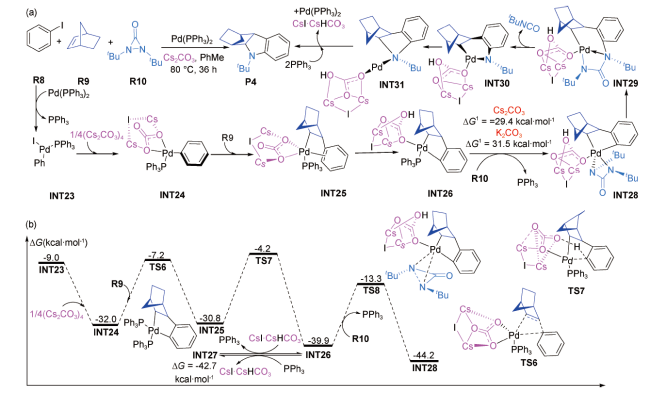
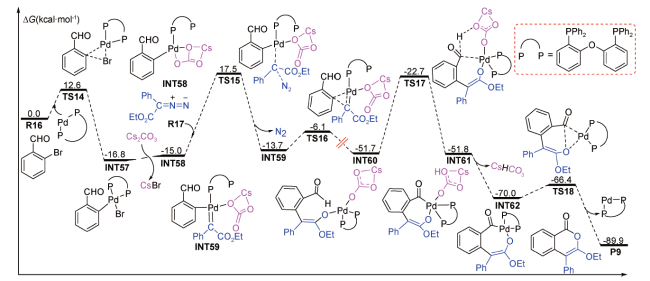
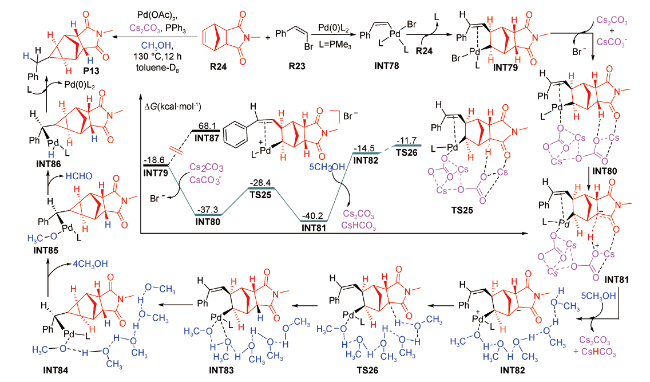
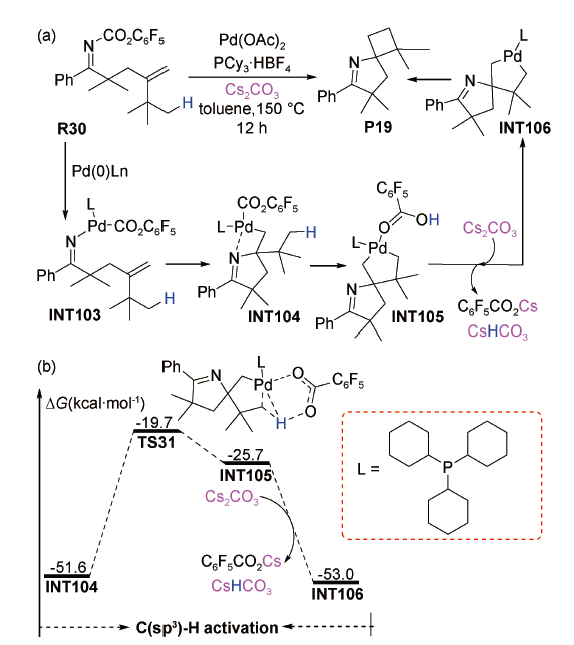
图式13 Cs2CO3辅助钯催化(Z)-2-溴乙烯基苯与endo-N-(对苯甲基)-降冰片烯琥珀酰亚胺[2+1]环加成的反应机理及其烷基C(sp3)—H活化的势能剖面图[93]Scheme 13 Reaction mechanism for Cs2CO3-assisted palladium-catalyzed [2+1] cycloaddition of (Z)-2-bromovinylbenzene with endo-N-(p-tolyl)-norbornene succinimide, and potential energy profiles for alkyl C(sp3)—H activation[93] |