1 引言
2 N2吸附和活化能力的提高
2.1 引入缺陷位点
表1 缺陷材料的光催化固氮性能Table 1 Photocatalytic nitrogen fixation performance of defective materials |
| Photocatalyst | Reaction medium | Light source | NH3 evolved | Defect type | Year | Ref. |
|---|---|---|---|---|---|---|
| a-MoO3-x NWs | Water | 300 W xenon lamp | 200.35 μmol·h-1·g-1 | OVs | 2023 | 18 |
| Zn-Co3O4 | Water | 300 W xenon lamp (λ ≥ 420 nm) | 96.8 μmol·h-1·g-1 | OVs | 2023 | 40 |
| SV-1T-MoS2 | Water+ Methanol | 300 W xenon lamp (AM 1.5G) | 8220.83 μmol·h-1·g-1 | SVs | 2020 | 44 |
| Bi2S3 | Water | 300 W xenon lamp | 51.04 μmol·L-1·h-1 | SVs | 2022 | 45 |
| NYF/NV-CNNTs | Water + Sacrificial agent | 300 W xenon lamp (λ ≥ 420 nm) | 1.72 mmol·L-1·g-1 | NVs | 2021 | 48 |
2.2 引入金属位点
表2 Fe掺杂材料的光催化固氮性能Table 2 Iron-doped materials for photocatalytic N2 fixation |
| Photocatalyst | Reaction medium | Light source | NH3 evolved | Year | Ref. |
|---|---|---|---|---|---|
| Fe-BiOCl | Water | 300 W xenon lamp | 30.00 μmol·L-1·h-1 | 2020 | 57 |
| Fe-BiOBr | Water | 300 W xenon lamp (λ≥ 420 nm) | 382.68 μmol-1·g-1·h-1 | 2020 | 60 |
| Fe-SrWO4 | Water | 300 W xenon lamp | 150.70 μmol·h-1·g-1 | 2020 | 61 |
| Fe0.05-CN | Water + Alcohol | 250 W high voltage sodium lamp | 5.40 mg·L-1·h-1·g-1 | 2017 | 62 |
| Fe-MCNC | Water + Methanol | 65 W LED | 1.88 μmol·h-1·g-1 | 2023 | 63 |
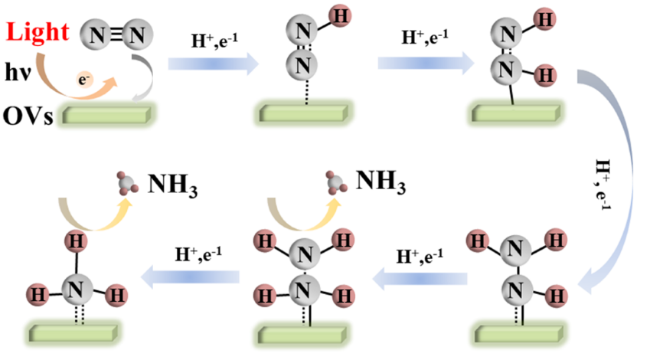
图2 (a) Ru1/2DAF的光生电子转移示意图[74]; (b) n型GaN NWs与金属Ru团簇形成肖特基势垒的示意图[76]; (c) 含氧空位的Ru负载TiO2纳米片上N2光还原机理图[77]Fig. 2 (a) Schematic diagram of photogenerated electron transfer in Ru1/2DAF[74]. (b) Schematic diagram for the formation of the Schottky barrier between n-type GaN NWs and metallic Ru clusters[76]. (c) Mechanistic diagram of N2 photoreduction over single Ru site loaded TiO2 nanosheets with oxygen vacancies[77] |
表3 Ru负载材料的光催化固氮性能Table 3 Photocatalytic nitrogen fixation of Ru supported materials |
| Photocatalyst | Reaction medium | Light source | NH3 evolved | Year | Ref. |
|---|---|---|---|---|---|
| Ru/W18O49 | Water | 300 W xenon lamp | 44.30 μmol·g-1·h-1 | 2023 | 30 |
| Ru1/2DAF | Water | 300 W xenon lamp | 213.00 μmol·g-1·h-1 | 2022 | 74 |
| Ru-MOF-74 | Water | 300 W xenon lamp (λ ≥ 420 nm) | 70.90 μmol·g-1·h-1 | 2022 | 75 |
| Ru@GaN | Hydrogen + Nitrogen | UV lamp 290-380 nm | 2400.00 μmol·g-1·h-1 | 2017 | 76 |
| Ru-TiO2 | Water + Alcohol | 300 W xenon lamp | 56.30 μg·h-1·g-1 | 2019 | 77 |
3 电荷转移能力的提升
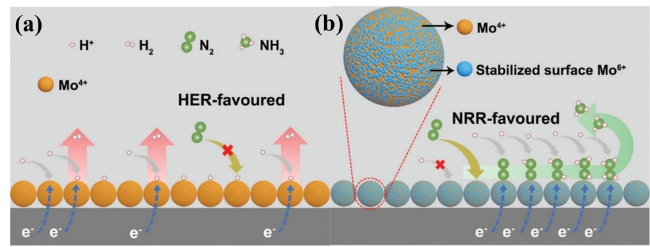
3.1 构建单金属混合价态催化剂
3.2 设计双金属位点催化剂
表4 双金属位点材料的光催化固氮性能Table 4 Bimetallic site materials for photocatalytic N2 fixation |
| Photocatalyst | Reaction medium | Light source | NH3 evolved | Year | Ref. |
|---|---|---|---|---|---|
| Fe/Mo-BMWO | Water | 300 W xenon lamp (λ ≥ 420 nm) | 218.93 μmol·h-1·g-1 | 2022 | 91 |
| CeF3:Yb3+, Er3+/Fe-ATP | Water | 300 W xenon lamp | 253.60 μmol·h-1·g-1 | 2022 | 92 |
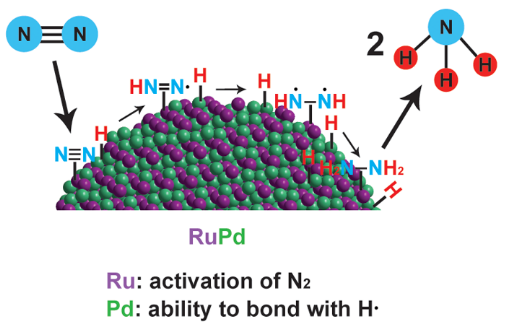
| RuPd/C3N4 | Water + Alcohol | 300 W xenon lamp | 1389.84 μmol·h-1·g-1 | 2021 | 93 |
| Ru-SA/ HxMoO3−y | Hydrogen + Nitrogen | 300 W xenon lamp (λ≥ 420 nm) | 4.00 mmol·h-1·g-1 | 2022 | 94 |
| RuO+Co/CoO | Water | 300 W xenon lamp (λ≥ 400 nm) | 306.00 μmol·h-1·g-1 | 2022 | 95 |