1 引言
2 金属-有机框架/水凝胶复合材料的制备
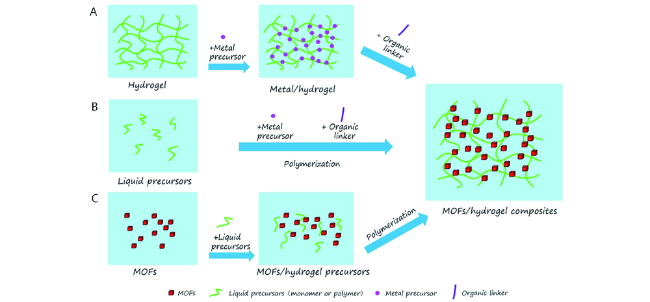
2.1 基于水凝胶MOFs原位生成法
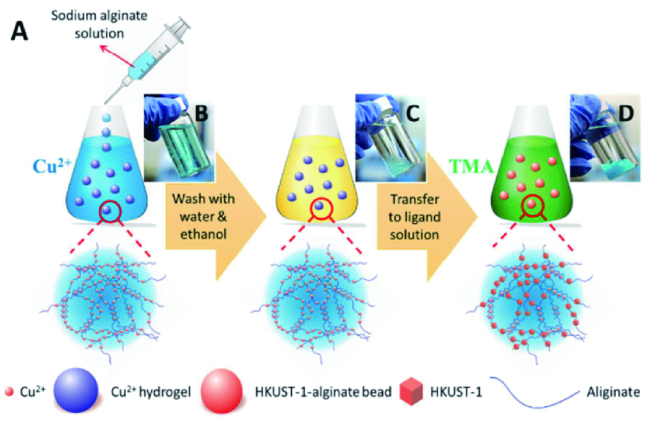
图2 (A) MOF -藻酸盐复合材料的制备原理图;(B)加入海藻酸钠溶液后,用Cu2+交联海藻酸水凝胶的照片;(C)用水和乙醇洗涤后的Cu2+交联海藻酸盐水凝胶;(D) HKUST -1-海藻酸水凝胶[27]Fig. 2 (A) Schematic of the preparation of MOF-alginate composite; Photographs of(B) alginate hydrogels cross-linked by Cu2+ right after the addition of sodium alginate aqueous solution into Cu2+ aqueous solution;(C) alginate hydrogels cross-linked by Cu2+ after washed with water and ethanol; and(D) HKUST-1-alginate hydrogels[27] |
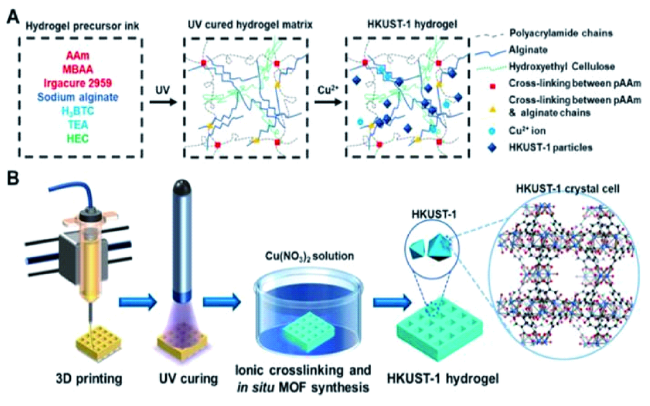
图3 化学组成原理图和3D打印工艺的MOF水凝胶结构。 (A)水凝胶前驱体油墨组成(左)、UV固化水凝胶基质(中)、HKUST-1水凝胶(右);(B)3D打印过程中三个关键步骤的示意图,包括打印、UV固化和离子交联[31]Fig. 3 Schematics of the chemical composition and 3D printing process for the MOF hydrogel structures.(A) Composition of the hydrogel precursor ink(left), UV-cured hydrogel matrix(middle), and the HKUST-1 hydrogel(right);(B) Schematic showing the three critical steps in the 3D printing process including printing, UV curing, and ionic cross-linking[31] |