Contents
1 引言
1.1 贵金属多孔纳米结构
1.2 有序贵金属多孔纳米结构
1.3 无序贵金属多孔纳米结构
2 贵金属多孔纳米结构的制备
2.1 硬模板法
2.2 软模板法
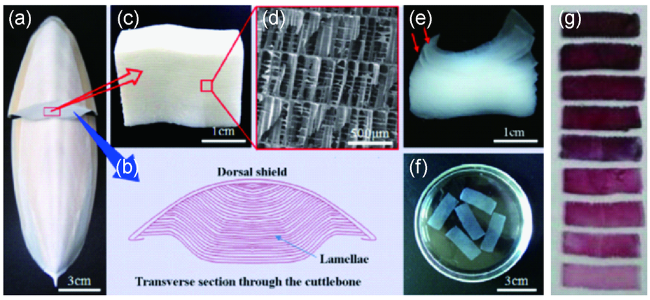
2.3 生物模板法
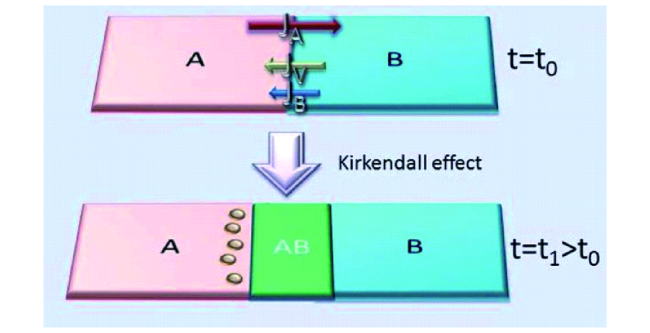
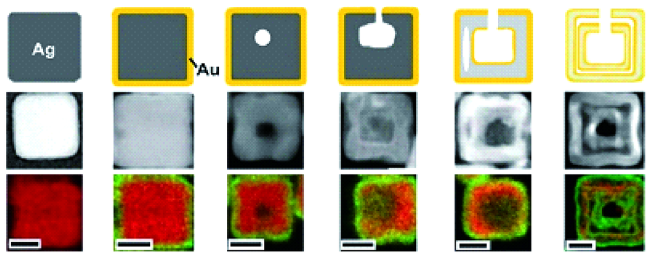
2.4 柯肯达尔效应
3 贵金属多孔纳米结构在生物检测中的应用
3.1 局域表面等离子共振(LSPR)
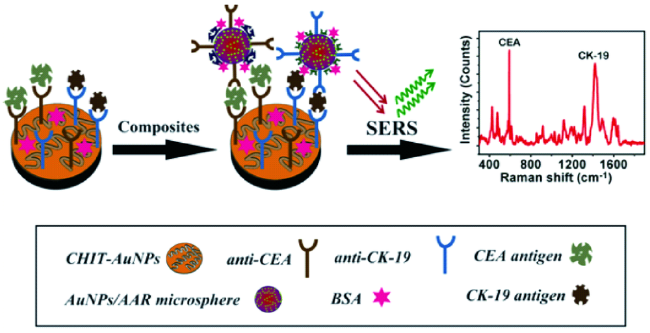
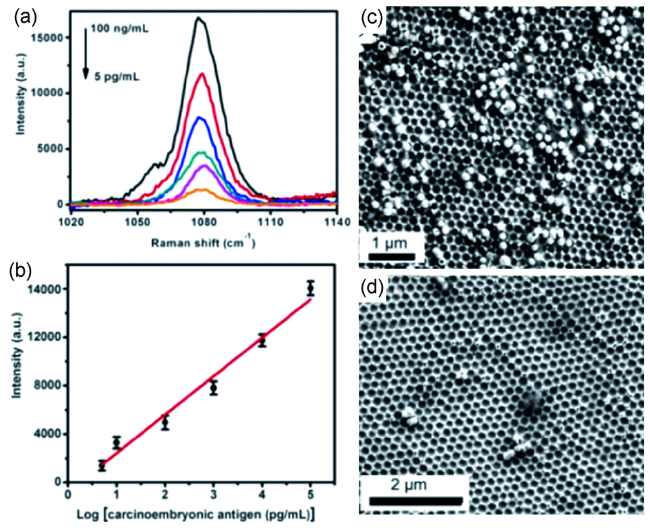
3.2 表面增强拉曼光谱(SERS)
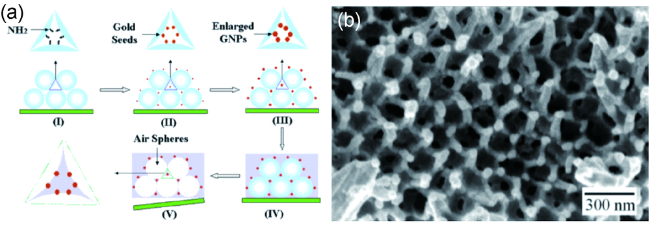
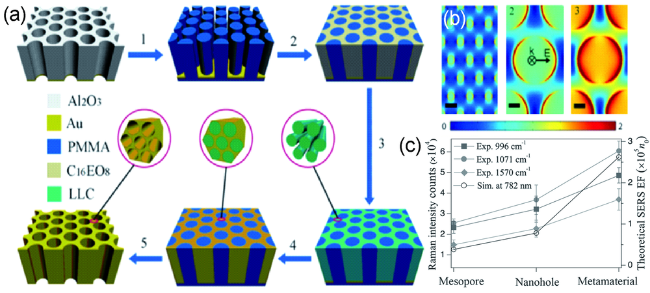
图13 (a)三维有序多孔Au纳米结构的制备过程,(b)产物表面的归一化电场振幅分布,(c)不同峰位置处的拉曼强度和电磁增强因子模拟[58]Fig. 13 (a) Synthesis procedure of 3D ordered porous Au nanostructures,(b) Normalized electric field(E-field) amplitude distribution at the surface,(c) Raman intensities at different peaks and the simulated EM enhancement factors[58] |